| RMO_CoursAnatomie et physiologie de cristallin |
Labyad.S ; Guechati.A ; Achergui.W ; Halhoul.A ; Boutaib.D ; Jabri.N ; Sekhsoukh.R
Université Mohammed Premier d’Oujda, Faculté de médecine et de pharmacie d’Oujda ; CHU Mohammed VI d’Oujda, Maroc ; Laboratoire d’Oto-Neuro-Ophtalmologie LRONO ;Reçu Le 27/10/2025 ; Accepté Le 08/11/2025 ; Disponible Sur Internet Le 09/11/2025 ; Doi
Plan
Définition ……………………………………………………………….
Embryologie ……………………………………………………………….
Anatomie descriptive…………………………………………………………………….
Forme générale………………………………………………………………….
Surfaces et repères…………………………………………………………….
Anatomie microscopique …………………………………………………………….
La capsule ………………………………………………………………….
L’épithélium antérieur………………………………………………………….
Les fibres cristalliniennes……………………………………………………….
Rapports ……………………………………………………………….
Vascularisation …………………………………………………………………….
Innervation …………………………………………………………………….
Système suspensif du cristallin ……………………………………………………….
Physiologie
Propriétés biochimiques et métaboliques ………………………………………
Propriétés physiques ………………………………………………………
Propriétés optiques ……………………………………………………………
Propriétés immunologiques : ………………………………………….
Propriétés cellulaire et renouvèlement cristallinien, homéostasie protéique et mécanismes de la cataractogenèse : …………………………………………
Conclusion …………………… ……………………………………………….
Définition :
Le cristallin est une lentille biconvexe, transparente et avasculaire, située en arrière de l’iris et en avant du vitré. Il est suspendu au corps ciliaire par la zonule de Zinn.
Sa puissance optique nette est d’environ +18 à +21 D, soit approximativement un tiers du pouvoir de convergence total de l’œil (la cornée apportant les deux tiers restants).
📍 Intérêt du cours :
- Clinique : rôle majeur dans l’acuité visuelle et la réfraction ; pathologies fréquentes (cataracte, subluxation) responsables d’altération visuelle réversible ou non.
- Pathologique : cataractes (nucléaire, corticale, sous-capsulaire antérieure/postérieure), traumatisme, anomalies congénitales, décollement/subluxation liée à laxité zonulaire (marfan, homocystinurie), opacités post-chirurgicales (opacification de la capsule postérieure).
- Physiologique : modèle pour l’étude de la différenciation cellulaire (cellules épithéliales antérieures → fibres cristalliniennes), de la protéomique (cristallines) et les mécanismes de transparence (homéostasie ionique, échanges avec l’humeur aqueuse).
- Chirurgical : extraction de cataracte et implantation d’implant intra-oculaire (IOL) ; interventions réfractives (phako-RLE, implantation de lentilles phakes) ; gestion des complications (capsulorhexis, vitrectomie, repositionnement d’IOL).
Embryologie :
Le développement du cristallin débute très tôt au cours de l’embryogenèse et résulte d’interactions complexes entre le neuroectoderme (vésicule optique), l’ectoderme de surface et la mésenchyme périoculaire (notamment dérivée de la crête neurale).
Vers le 22ᵉ jour du développement embryonnaire, des replis au niveau du prosencéphale donnent naissance aux sillons (gouttières) optiques, qui s’évasent ensuite pour former les vésicules optiques (issues du neuroectoderme). Le col étroit de ces vésicules les relie encore au cerveau antérieur en développement.
Lorsque la vésicule optique entre en contact avec l’ectoderme de surface, elle s’invagine pour former la cupule optique bilaminaire. Cette invagination de la vésicule coïncide avec l’induction du cristallin au niveau de l’ectoderme de surface.
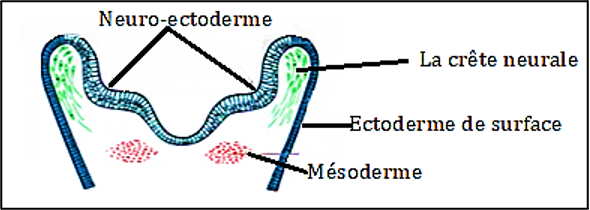
- Induction et formation du cristallin :
Le contact entre la vésicule optique et l’ectoderme de surface déclenche une cascade d’événements moléculaires (facteurs comme PAX6, FGF, BMP, entre autres) qui stimulent la prolifération et l’épaississement local de l’ectoderme pour former la plaque cristallinienne (placoide cristallinienne).
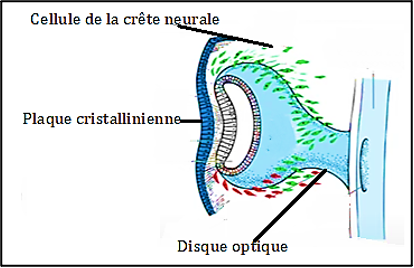
La placode s’invagine ensuite pour former la fossette cristallinienne, puis se ferme et se détache de l’ectoderme de surface pour donner la vésicule cristallinienne. Les cellules résiduelles de l’ectoderme de surface au-dessus de la vésicule cristallinienne se différencient pour former l’épithélium cornéen primitif.
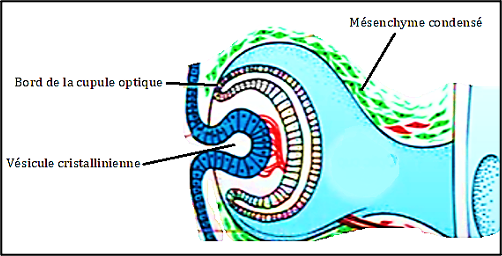
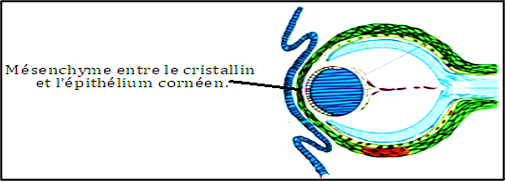
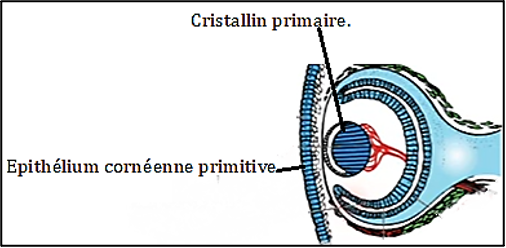
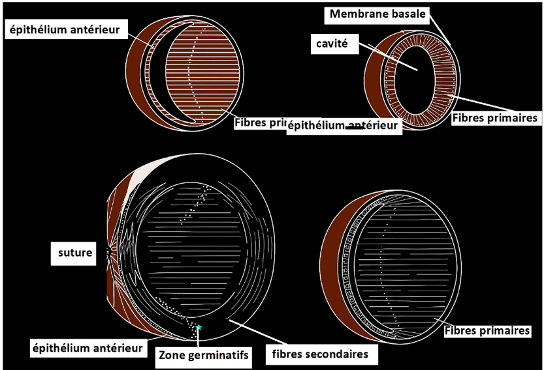
La vésicule cristallinienne se différencie selon une organisation asymétrique : les cellules du pôle postérieur s’allongent en fibres primaires qui comblent la vésicule et forment le noyau primitif, tandis que les cellules du pôle antérieur restent épithéliales et donneront ultérieurement les fibres secondaires. La formation des fibres primaires commence peu après la fermeture de la vésicule (fin du 1ᵉʳ mois / début du 2ᵉ mois embryonnaire chez l’humain), alors que la production de fibres secondaires se poursuit tout au long de la vie, expliquant la croissance concentrique du cristallin.
Ce processus est orchestré par un réseau moléculaire (notamment PAX6, SOX2, FGF, voies BMP/TGF-β, Wnt, Notch) qui régule la prolifération, l’invagination, la polarité et la différenciation des cellules de la placode pour aboutir à un cristallin transparent, avasculaire et fonctionnel.
Anatomie descriptive
Forme générale :
- Lentille biconvexe (face postérieure plus bombée).
- Diamètre équatorial : 6,5 mm à la naissance → 9 mm à l’âge adulte.
- Épaisseur axiale : 3.5 – 4 mm à la naissance → 4–5 mm à l’âge adulte (augmente lentement avec l’âge).
- Poids : 65-70 mg à la naissance → 200–220 mg vers 60 ans.
- Puissance optique : +18 à +22 D (varie avec l’âge et l’accommodation, l’indice et l’accommodation).
- Rayons de courbure : face antérieure 10 mm au repos (devient plus convexe en accommodation≈ 6–7 mm) ; face postérieure 6 mm (varie peu).
- Indice de réfraction : gradient trans-cristallinien (valeur moyenne centrale 1,40–1,42), expliquant la contribution optique sans fortes aberrations.
- Couleur : cristallin jeune habituellement incolore ; brunissement et ambrage apparaissent avec l’âge.
Surfaces et repères :
- Faces : antérieure et postérieure, reliées latéralement par l’équateur.
- Pôles : antérieur et postérieur = centres géométriques des faces.
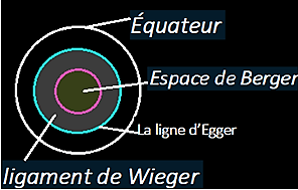
- Équateur : zone d’insertion de la zonule de Zinn qui suspend le cristallin.
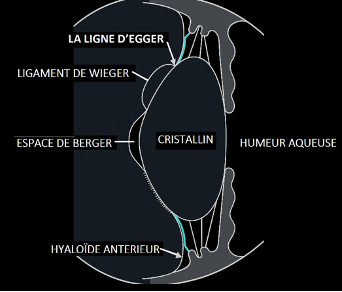
- Espace de Berger / ligament de Wieger : adhérence circulaire entre la capsule postérieure du cristallin et la face antérieure du corps vitré. La ligne d’Egger peut être décrite comme le bord de cette zone d’adhérence.
Anatomie microscopique :
LA CAPSULE:
- Membrane basale épaisse synthétisée par l’épithélium antérieur.
- La capsule joue le rôle de barrière métabolique et pourrait intervenir dans le modelage du cristallin lors de l’accommodation.
- Son épaisseur varie selon les zones ; aux régions les plus épaisses, la capsule représente la membrane basale la plus épaisse de l’organisme. La plus grande épaisseur de la capsule antérieure (12–14 μm) par rapport à la capsule postérieure (3–6 μm). Beaucoup plus fine, s’explique en partie parce que l’épithélium, qui sécrète activement la capsule, est en contact direct de la face antérieure, alors qu’il est absent sur la face postérieure.
💡 Note : Ces différences locales d’épaisseur ont une importance chirurgicale, notamment en raison du risque de déchirure ou de rupture de la fine capsule postérieure lors de la chirurgie de la cataracte.
- Composition : collagène type IV, laminines, fibronectine… → élasticité remarquable et rôle de barrière sélective ; point d’ancrage de la zonule.
💡 Note : Des vestiges de la tunica vasculosa lentis sont fréquents et apparaissent comme des opacités gris clair (points de Mittendorf) au niveau ou à proximité du pôle postérieur ; ces opacités sont rarement responsables d’une perte visuelle significative.
L’ÉPITHÉLIUM ANTÉRIEUR SUBCAPSULAIRE
- Épithélium simple unistratifié, se limite à la face antérieure et au bourrelet équatorial du cristallin.
- On peut distinguer biologiquement en deux zones comportant deux types cellulaires différents :
- Cellules centrales aplaties (Cellules A) : relativement quiescentes, à faible activité mitotique.
💡 Note :
- Dans diverses pathologies (inflammation, traumatisme), la réponse principale de ces cellules antérieures est la prolifération et la transformation fibreuse (métaplasie fibreuse), conduisant à la formation de tissu fibrotique (former une plaque épithéliale sous-capsulaire antérieure).
- Récemment, une complication potentielle a été mise en évidence en chirurgie réfractive : les opacités sous-capsulaires antérieures décrites après implantation d’implants phakes dans la chambre postérieure en position proche ou en appui sur la surface antérieure du cristallin —> la prolifération des cellules A et réponse fibrotique.
- Zone germinative/pré-équatoriale (Cellules E) : zone mitotique majeure ; près de l’équateur, cellules cubiques → se différencient en fibres.
- Rôle : production continue de fibres secondaires, maintenance des échanges, synthèse de la capsule.
💡 Note :
- En situation pathologique, les cellules E ont tendance à migrer vers la capsule postérieure ; au lieu de subir une transformation fibreuse, elles forment des cellules volumineuses en « ballonnets » (cellules de Wedl), visibles cliniquement comme des « perles ». Ces cellules équatoriales sont la source principale de la cataracte secondaire classique, en particulier de la forme en « perles » de l’opacification capsulaire postérieure « Elschnig’s Pearls »
- Les cellules E sont également impliquées dans la formation de l’anneau de Soemmering, lésion en forme d’anneau (donut) composée de cortex cristallin retenu/régénéré et de cellules, qui peut survenir après toute interruption de la capsule antérieure (initialement décrite en rapport avec un traumatisme oculaire).
Les FIBRES CRISTALLINIENNES= Substratum de cristallin
® Le cristallin croît de l’intérieur vers l’extérieur : les fibres les plus anciennes (formées précocement) occupent le noyau central, tandis que les fibres récentes constituent le cortex périphérique. Cette architecture produit un gradient d’âge cellulaire et des propriétés biomécaniques/optique variables du centre vers la périphérie.
1. Noyau :
Le noyau rassemble des fibres formées aux stades précoces et se subdivise classiquement en sous-zones selon l’âge des fibres :
Noyau embryonnaire : fibres primaires (ISSUES DES CELLULES POSTERIEURES de la vésicule cristallinienne qui se sont allongées tôt pendant l’embryogenèse).
Noyau fœtal : fibres secondaires formées in utero.
Noyau juvénile / adulte : fibres formées respectivement après la naissance et à la puberté/maturité.
Les fibres du noyau sont densément empaquetées, dénucléées et dépourvues d’organites ; avec l’âge elles subissent condensation et brunissement (sclérose).
2. Cortex cristallinien :
- Couches périphériques constituées des fibres les plus récentes.
- Organisation pratique : on parle classiquement de cortex superficiel / intermédiaire / profond, mais ces subdivisions sont avant tout descriptives et quelque peu arbitraires.
- Rôle : le cortex confère flexibilité et continue d’accroître la puissance/masse du cristallin ; il est le siège des modifications liées à la presbytie et aux cataractes corticales.
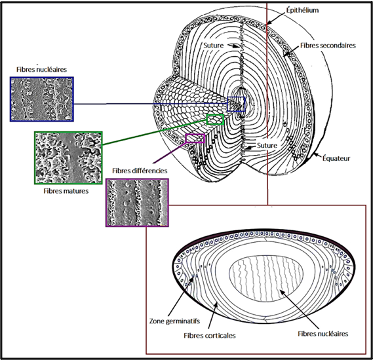
💡 Microstructure et formation des fibres cristalliniennes :
| A. FIBRES PRIMAIRES : Proviennent des cellules du pôle postérieur de la vésicule cristallinienne qui, après fermeture, s’allongent en fibres primaires.Très longues, orientées essentiellement selon l’axe antéro-postérieur, de section variable. Elles constituent le noyau embryonnaire. Les fibres primaires, formées tôt in utero, n’ont pas une organisation en couches régulières comme le cortex; elles ne forment pas de sutures complexes initialement. b. fibres secondaires Mitoses de l’épithélium antérieur dans la zone pré-équatoriale (zone germinative).Différenciation : les cellules filles migrent vers l’équateur, s’allongent, perdent leur noyau et la plupart des organites, synthétisent massivement les cristallines et deviennent fibres secondaires.Croissance : les fibres secondaires s’ajoutent en couches concentriques autour du noyau, assurant la croissance continue du cristallin tout au long de la vie.Rotation / réorientation de la polarité cellulaire :Lors de la transformation en fibre, la polarité apico-basale de la cellule s’inverse/roque d’environ 90° : l’ancien pôle apical se retrouve dirigé vers l’une des extrémités de la fibre.Ce réarrangement permet d’aligner les extrémités des fibres vers les pôles et d’obtenir une architecture apicale/basale cohérente, essentielle à la formation des sutures et à la compaction fibreuse. |
Les fibres secondaires du cristallin forment une architecture tridimensionnelle complexe : elles ne sont pas de simples méridiens reliant directement les pôles antérieur et postérieur, mais suivent des trajets courbes et s’emboîtent pour construire le cortex et les sutures. Deux morphotypes coexistent et s’organisent en réseaux imbriqués :Fibres « droites » (crescent-shaped / croissantées)Ce sont des segments courbés dont la conformation générale évoque un croissant ; à l’embryogenèse, elles peuvent s’organiser en faisceaux compacts (packing souvent hexagonal) permettant une compaction régulière du tissu. Fibres en « S » tridimensionnel (3D S-shape)Chaque fibre présente une double courbure : une courbure principale convexo-concave (donnant l’aspect de croissant sur la longueur), et une inflexion aux extrémités : les segments terminaux se courbent en sens opposé par rapport à l’axe polaire.Ce profil en S permet aux extrémités des fibres de s’abutter et de chevaucher formant ainsi les branches de suture (antérieure et postérieure).
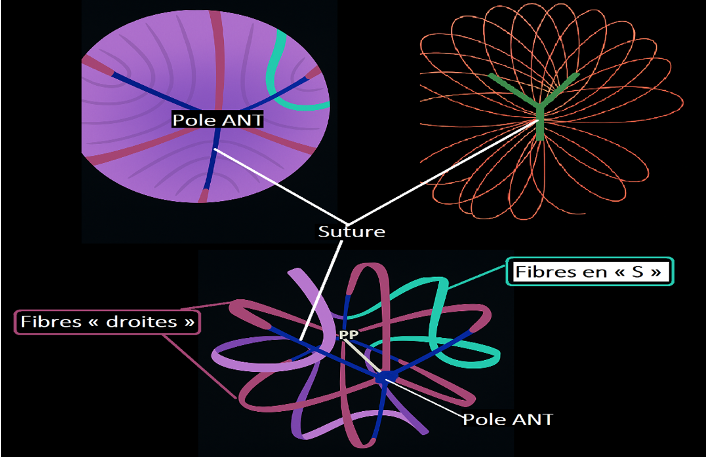
3. Sutures :
Les extrémités des fibres (droites et en S) s’abuttent et se chevauchent en arcs latitudinaux ; ces jonctions forment les branches de suture.
- Type :
- Suture antérieure : réunion des faces apicales des fibres.
- Suture postérieure : réunion des faces basales.
- Morphogenèse :
- Les fibres secondaires formées in utero produisent des sutures en Y : antérieurement un Y droit, postérieurement un Y inversé.
- Avec la croissance postnatale, les sutures deviennent de plus en plus complexes et ramifiées (multiplication des branches) :
Enfance → 3–6 branches,
Adolescence → 6–9 branches,
Âge adulte/sénescence → jusqu’à 9–15 branches complexes.
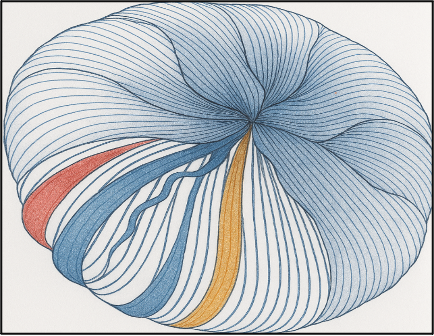
- Rôle optique :
La complexification progressive des sutures contribue à la distribution homogène de la lumière et limite les artefacts de diffusion, participant ainsi à la bonne qualité optique du cristallin.
Rapports
Antérieurs :
L’iris, percé par la pupille, constitue la limite antérieure de la chambre postérieure : cette chambre est délimitée en avant par l’iris, en arrière par le cristallin et latéralement par le corps ciliaire.
En avant de l’iris se trouve la chambre antérieure, bordée antérieurement par la cornée. La profondeur de la chambre antérieure centrale chez l’adulte est de l’ordre de 3,0–3,6 mm (valeur variable selon l’âge et la réfraction).
Postérieurs :
La face postérieure du cristallin est en relation intime avec la face antérieure du vitré. Une adhérence fibreuse circulaire, l’anneau (ou ligament) de Wieger, fixe la membrane hyaloïdienne antérieure à la capsule postérieure du cristallin et délimite en avant l’espace de Berger (espace virtuel rétro-lenticulaire).
En périphérie, l’équateur du cristallin s’articule fonctionnellement avec la zonule de Zinn (faisceaux zonulaires issus du corps ciliaire).
Vascularisation :
1. AVASCULARITE PHYSIOLOGIQUE
Le cristallin mature est avasculaire (absence d’artères, veines et lymphatiques intra parenchymateuses) ; condition nécessaire à sa transparence. La capsule est une membrane basale mais non vascularisée.
2. VASCULARISATION EMBRYONNAIRE (TRANSITOIRE)
Au cours du développement fœtal, le cristallin est alimenté par la TUNICA VASCULOSA LENTIS (réseau vasculaire autour du cristallin) et l’artère hyaloïde qui pénètrent la cavité vitréenne.
La régression normale de ce système (remodelage vasculaire) aboutit à l’avasculaireité du cristallin.
💡 Note : Échec de régression → persistance de membranes pupillaires ou persistance du vitré primitif hyperplasique, pouvant causer une opacité lenticulaire et des anomalies oculaire
Innervation :
1. ABSENCE D’INNERVATION PROPRE
Le cristallin n’est pas innervé : pas de fibres sensorielles ou autonomes intraparenchymateuses. Il est cependant en contact étroit avec des tissus richement innervés.
2. INNERVATION FONCTIONNELLE INDIRECTE (STRUCTURES VOISINES)
- Muscle ciliaire : innervation parasympathique par le noyau d’Edinger-Westphal → nerf oculomoteur → ganglion ciliaire → fibres ciliaires courtes. La contraction du muscle ciliaire modifie la tension zonulaire et donc la forme du cristallin (accommodation).
- Innervation sensorielle et trophique : les fibres sensorielles du nerf trijumeau (V1) innervent la conjonctive, le limbe et la région périciliaire ; elles participent indirectement à la trophicité oculaire. Les terminaisons nerveuses libèrent neuropeptides (NGF, substance P, CGRP) pouvant moduler la santé épithéliale et la régulation locale mais sans innervation directe du parenchyme cristallinien.
Système suspensif du cristallin :
Le système suspensif (zonule de Zinn et faisceaux associés) assure la centration du cristallin et la transmission des forces d’accommodation générées par le muscle ciliaire.
Il se compose de structures capsulaires, vitréennes et zonulaires étroitement intégrées.
1. Position et attaches postérieures du cristallin
Le pôle postérieur du cristallin siège dans la fosse hyaloïdienne, une légère dépression de la face antérieure du corps vitré.
La membrane hyaloïdienne antérieure adhère à la capsule postérieure du cristallin par un anneau fibreux circonférentiel appelé ligament (ou anneau) de Wieger, qui borde en avant l’espace de Berger.
Le bord périphérique de cette attache, parfois visible en chirurgie ou en imagerie, est désigné comme la ligne (ou cercle) d’Egger.
Ces structures constituent une interface anatomique et fonctionnelle entre le cristallin et le vitré antérieur, participant à la stabilité postérieure du cristallin.
2. Origine, trajets et classification des fibres zonulaires
Les fibres zonulaires émergent du corps ciliaire selon plusieurs faisceaux anatomiques et fonctionnels :
- ZONULE DE LA PARS PLANA :
Les fibres naissent principalement des baies de la pars plana (pars orbicularis), cheminent en avant le long de la pars plana puis vers les vallées inter-processus ciliaires. Elles sont initialement fines et se rassemblent en faisceaux plus épais en direction du cristallin.
- ZONULE DE LA PARS PLICATA :
Fibres prenant origine aux bases et sommets des processus ciliaires (pars plicata) et se dirigeant directement vers la capsule cristallinienne.
- ZONULE HYALOÏDIENNE (VITREOUS ZONULE) :
Faisceaux reliant les procès ciliaires à l’hyaloïde antérieure (près du ligament de Wieger) ou longeant la surface vitréenne antérieure.
Ce système assure la continuité fonctionnelle entre le vitré, la zonule et le cristallin.
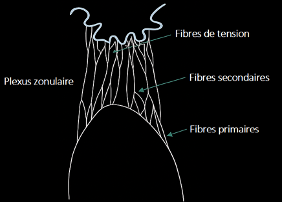
3. Organisation du plexus zonulaire
Les différents faisceaux se rejoignent dans une région de convergence appelée plexus zonulaire, où ils se croisent, se regroupent et se redistribuent avant leur insertion capsulaire.
On distingue :
- Des fibres primaires, rejoignant directement la capsule cristallinienne ;
- Des fibres secondaires ou d’interconnexion, reliant entre eux les faisceaux du plexus ;
Certaines séries décrivent des fibres de tension courtes ancrant le plexus aux parois des procès ciliaires.
La configuration de ce réseau varie selon les études, mais son organisation en grillage tridimensionnel permet de concilier stabilité du cristallin et mobilité fine indispensable à l’accommodation.
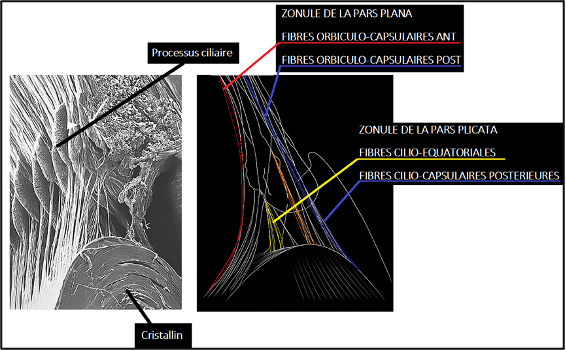
4. Topographie d’insertion des fibres zonulaires
L’insertion des fibres zonulaires sur la capsule cristallinienne suit une organisation topographique régulière, reflétant l’origine segmentaire des faisceaux ciliaires et leur intégration dans un plexus zonulaire périciliaire.
A. Fibres d’origine pars plana — les fibres orbiculo-capsulaires
Les faisceaux issus de la pars plana (pars orbicularis) constituent les fibres dites ORBICULO-CAPSULAIRES. Après un trajet antéro-médian le long de la pars plana, ces fibres se répartissent en deux branches principales au voisinage du plexus zonulaire :

- FIBRES ORBICULO-CAPSULAIRES ANTERIEURES : s’insèrent sur la capsule antérieure cristallinienne (région antéro-équatoriale / pré-équatoriale).
- FIBRES ORBICULO-CAPSULAIRES POSTERIEURES : se dirigent vers la face postérieure de la capsule, avec un point d’insertion situé légèrement en arrière du ligament de Wieger (sur une coupe transversale).
💡 Note : Cette double distribution explique pourquoi certaines perturbations zonulaires peuvent affecter sélectivement la sustentation antérieure ou postérieure du cristallin.
B. Fibres d’origine pars plicata — les fibres cilio-équatoriales et cilio-capsulaires
Les fibres issues de la pars plicata (processus ciliaires) se distinguent également selon leur point d’origine et leur terminaison :
- FIBRES CILIO-EQUATORIALES : issues des sommets des processus ciliaires, elles se terminent principalement au niveau équatorial de la capsule (zone d’insertion dite équatoriale).
- FIBRES CILIO-CAPSULAIRES POSTERIEURES : naissant des vallées inter-processus ciliaires, elles se dirigent vers la capsule postérieure et contribuent à l’attache post-équatoriale du cristallin.
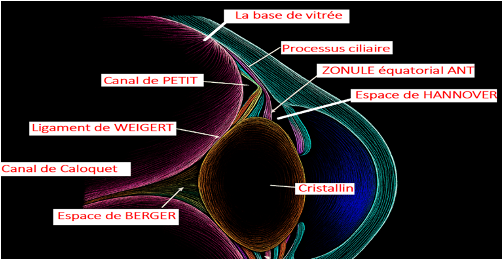
C. Espaces péri-zonulaires (terminologie historique)
La littérature anatomique mentionne classiquement des espaces péri-zonulaires tels que le canal de Hannover (zone comprise entre zonules pré- et post-équatoriales) et le canal de Petit (espace situé entre les zonules post-équatoriales et l’hyaloïde antérieure). Ces appellations sont d’intérêt historique et topographique ; leur description exacte varie selon les séries anatomiques et leur usage est moins fréquent dans les descriptions modernes mais reste utile pour la lecture des anciens traités et pour la compréhension des rapports péri-zonulaires en chirurgie antérieure.
5. Zone d’insertion capsulaire (implantation zonulaire)
La bande d’implantation zonulaire sur la capsule cristallinienne est située autour de l’équateur et s’étend classiquement sur une largeur d’environ 1–1,5 mm (valeurs variables selon les auteurs). Histologiquement, cette région se caractérise par :
- Une zone de fibres capsulaires plus denses (parfois décrite comme lamelle zonulaire) favorisant l’adhérence mécanique des fibrilles zonulaires à la capsule ;
- Une capsule qui, à ce niveau, présente des propriétés mécaniques adaptées à la transmission des forces zonulaires.
💡 Note : La connaissance précise de cette topographie est essentielle en chirurgie de la cataracte (repérage des insertions zonulaires, mise en place d’anneaux de tension capsulaire, fixation d’implants scléraux) et en prise en charge des luxations/subluxations cristalliniennes.
Les lésions de la zone équatoriale (traumatisme, pseudo-exfoliation, pathologies congénitales) exposent au risque de faiblesse zonulaire et de complications per-opératoires (swinging nucleus, rupture capsulaire, dislocation d’IOL).
Physiologie :
Le cristallin et son système suspensif (zonule de Zinn) constituent une unité fonctionnelle essentielle à la réfraction et à l’accommodation. Leur fonctionnement optimal repose sur des propriétés biochimiques, métaboliques, physiques, mécaniques et immunologiques finement coordonnées. La compréhension de ces mécanismes éclaire les processus de vieillissement lenticulaire et la pathogenèse de la cataracte.
I – PROPRIETES BIOCHIMIQUES ET METABOLIQUES :
1. Protéines du cristallin — composition et rôles:
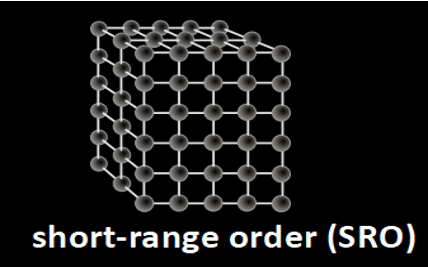
Le cristallin concentre une très forte proportion de protéines (33 %), c’est l’un des tissus les plus riches en protéines de l’organisme, et ces protéines conditionnent sa short-range order (SRO), sa transparence et son indice de réfraction.
Répartition protéique :
- Fraction soluble : 80–90 % du total protéique (principalement les cristallines)
- Fraction insoluble (protéines membranaires et agrégats) : 10–20 % (augmente avec l’âge)
- Les Zonules : microfibrilles composées principalement de fibrilline-1 et de glycoprotéines associées, conférant résistance mécanique et élasticité. Transport :
Cristallines (α, β, γ, majoritaires dans la fraction soluble)
- α-cristallines (αA, αB) : chaperonnes moléculaires (small heat-shock proteins) ; forment des oligomères dynamiques qui limitent l’agrégation des autres protéines. Rôle crucial pour la stabilité optique. Leur fonction chaperonne décroît avec l’âge et après certaines Modifications post-traductionnelles PTM.
- Les α et β sont constituées de sous-unités ; leur assemblage/agrégation conditionne les propriétés physico-chimiques et la transparence.
Rôle de la fraction insoluble (les albuminoïdes) :
sont des protéines membranaires, agrégats covalents et produits de PTM (cross-links). Leur proportion augmente avec l’âge, mais leur seule présence n’explique pas la cataracte : c’est la nature et l’organisation de ces agrégats qui rendent la lumière diffuse.
Synthèse protéique :
La synthèse protéique (ARN, traduction) est localisée à l’épithélium antérieur et à la zone équatoriale : ce sont ces cellules qui produisent protéines et membranes nécessaires à la différenciation des fibres. Les fibres matures perdent leur noyau et organites — elles ne synthétisent plus de protéines.
Les acides aminés nécessaires à la synthèse protéique sont transportés activement par l’épithélium antérieur. Il existe trois pompes distinctes pour les acides aminés acides, basiques et neutres. Une fois incorporés, ces acides aminés sont métabolisés et servent aussi de source d’énergie.
2. Métabolisme énergétique et voies glucidiques :
a) Substrats et échanges :
- Le Cristallin avasculaire : dépend du glucose diffusant depuis l’humeur aqueuse (5,5 mmol·L⁻¹ dans l’humeur aqueuse vs 1 mmol·L⁻¹ dans le cristallin).
- Transporteurs de glucose : GLUT1 est le principal transporteur exprimé à l’épithélium/zone équatoriale.
b) Voies énergétiques :
- Glycolyse anaérobie : majoritaire (80 % du glucose utilisé) → production d’ATP et de lactate.
- Shunt des pentoses : 15 % : produit NADPH (indispensable pour maintenir le GSH réduit) et fournit des pentoses pour la synthèse d’ARN.
- Cycle de Krebs / phosphorylation oxydative : faiblement utilisé (peu de mitochondries ; consommation d’O₂ très faible).
- Voie des polyols (sorbitol) : faible en conditions normales ; 💡 Note : devient pathologique en hyperglycémie (aldose réductase- enzyme abondante- convertit glucose → sorbitol, la faible activité de sorbitol déshydrogénase favorisant l’accumulation de sorbitol) → cataracte diabétique.
c. Fonctions énergétiques
- ATP est nécessaire pour le transport actif d’ions, le maintien de la déshydratation (transports osmotiques), et la synthèse protéique dans les zones épithéliales/équatoriales.
3. Métabolisme lipidique :
Composition lipidique :
- Lipides = 3–5 % du poids sec du cristallin.
- Cholestérol 50 % des lipides (25 % du cholestérol total peut être sous forme estérifiée).
- Phospholipides 45 % (notamment riche en sphingomyéline).
- Glycosphingolipides / céramides 5 %.
Rôles :
- Rapport cholestérol/phospholipides extrêmement élevé → membranes plus rigides (résistance mécanique).
- Lipides structurent les membranes des fibres et interagissent avec les protéines membranaires et les cristallines ; l’altération lipidoprotéiques perturbent la compaction et la SRO → risque d’insolubilisation protéique et de cataracte.
💡 Note : Des cataractes ont été observées chez l’homme après traitement par des agents antihypercholestérolémiants tels que le triparanol. Les données sur statines modernes restent moins nettes.
4. Acide ascorbique (vitamine C) et défenses antioxydantes
- Concentration : l’acide ascorbique est plus concentré dans le cristallin que dans l’humeur aqueuse.
- Rôle : antioxydant ; peut participer aux réactions d’élimination des peroxydes, en partie couplé au glutathion (GSH).
II- PROPRIÉTÉS PHYSIQUES DU CRISTALLIN :
1) Viscoélasticité :
Le cristallin se comporte comme un matériau viscoélastique : il peut se déformer sous l’effet d’une force puis retrouver sa forme initiale, mais avec un léger retard.
Avec l’âge, il perd progressivement sa souplesse (sclérose nucléaire), augmente en rigidité et devient moins apte à modifier sa courbure : c’est le mécanisme principal de la presbytie
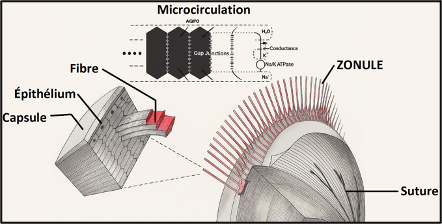
2) Appareil zonulaire :
Le réseau des microfibrilles zonulaire assure :
® La transmission des forces d’accommodation,
® La stabilité et la centration du cristallin dans le sac capsulaire.
3) Mécanique de l’accommodation (théorie de Helmholtz) :
La contraction du muscle ciliaire → relâchement de la tension zonulaire.
La capsule élastique permet alors au cristallin de se bomber, surtout sur sa face antérieure.
→ La puissance dioptrique augmente, permettant la vision de près.
💡 Note : Avec l’âge (presbytie) :
§ Diminution de l’élasticité du cristallin,
§ Éventuellement altérations de la zonule → baisse progressive de l’amplitude accommodative.
III —PROPRIÉTÉS OPTIQUES :
A –transparence :
Le cristallin transmet la lumière sans diffusion ni distorsion afin de projeter une image nette sur la rétine.
Cette transparence repose sur :
- Un SHORT-RANGE ORDER (SRO) : organisation locale et régulière des cristallines entraînant une annulation des diffusions lumineuses par interférences destructrices ;
- Un CYTOPLASME GELIFIE stabilisant cette organisation ;
- Le CONTROLE PRECIS de l’hydratation, du pH et des protéines solubles.
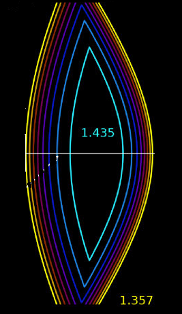
B – Réfraction :
Avec la cornée, le cristallin forme la « REFRACTON OCULAIRE ».
Il possède :
- Une forte concentration en cristallines, générant un indice réfractif élevé,
- Un gradient d’indice réfractif (GRIN) : plus élevé au noyau qu’en périphérie, ce qui réduit les aberrations sphériques et améliore la focalisation.
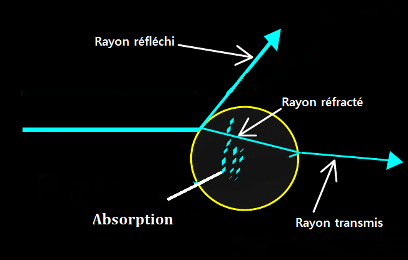
C- Réflexion
À chaque changement d’indice (lois de Fresnel), une fraction de la lumière est réfléchie.
Le cristallin limite ces pertes grâce à :
- Une transition douce des indices entre humeur aqueuse → cristallin → vitré,
- L’absence d’interfaces internes nettes (grâce au gradient d’indice progressif).
D- Absorption
- Faible dans le spectre visible,
- Augmente dans les UV : rôle protecteur vis-à-vis de la rétine.
Les protéines, pigments et l’acide ascorbique participent à cette absorption.
Avec l’âge, des dépôts (chromophores, lipofuscine) s’accumulent et diminuent la transmission lumineuse.
IV — PROPRIÉTÉS IMMUNOLOGIQUE ET PRIVILÈGE IMMUNITAIRE
La cornée est un organe à la fois exposé (contact direct avec l’environnement) et hautement protégé . Elle doit donc concilier deux besoins contradictoires : défendre contre les microbes et réparer les lésions, tout en évitant une inflammation destructrice qui briserait l’ordre stromal et altérerait la vision.
1 -Défenses de première ligne : barrières physiques et biochimiques
1.1 Protéines antimicrobiennes et facteurs solubles
- Film lacrymal : Contient IgA sécrétoire, lysozyme, lactoferrine, lipocaline, surfactant proteins et facteurs tensioactifs.
- Épithélium produisent défensines (β-defensins)
- Rôle : neutralisation microbienne, limitation de l’adhésion, actions bactéricides.
1.2 Épithélium cornéen et glycocalyx
- Épithélium multicouche formant barrière physique ; jonctions serrées et renouvèlement cellulaire rapide.
- Glycocalyx / mucines membranaires : empêchent la colonisation.
2 – Immunité innée cornéenne : détection et réponse rapide
2.1 Récepteurs de détection (PRR)
Les cellules de surface (épithélium, cellules immunes résidentes) possèdent des capteurs qui reconnaissent des signaux microbiaux typiques (PAMPs).
Quand ces capteurs détectent un intrus, ils déclenchent immédiatement la production de médiateurs inflammatoires et de peptides antimicrobiens.
→ Signal d’alerte rapide qui attire et active les défenses (neutrophiles, macrophages).
2.2 Les effecteurs rapides :
- Neutrophiles : les premiers arrivés ; phagocytent, tuent les microbes et piéger les germes.
- Macrophages / monocytes : nettoient, sécrètent des cytokines et aident à présenter l’antigène pour la suite de la réponse.
- Cellules dendritiques immatures : surveillent surtout le limbe ; en cas d’alerte elles mûrissent, montent au ganglion et présentent l’antigène aux lymphocytes.
2.3 CPA résidentes :
- Cornée centrale normale : très peu d’CPA « actives » → tolérance locale.
- Périphérie / limbe : riche en cellules immunitaires (CD immatures, macrophages) prêtes à réagir.
- En cas d’inflammation : les CPA s’activent, migrent via de nouvelles voies lymphatiques et lancent la réponse adaptative (activation des lymphocytes T dans les ganglions).
3 – Le privilège immunitaire : mécanismes locaux et systémiques
Le cristallin bénéficie d’un isolement immunologique relatif (absence de vascularisation, capsule comme barrière).
L’exposition antigénique peut déclencher des réponses inflammatoires. Le milieu aqueux et le privilège immunitaire antérieur contribuent à limiter les réponses destructrices.
® Uvéite Phacoantigénique (ou phacoanaphylactique) : réaction immunitaire auto-immune contre les antigènes du cristallin libérés après rupture capsulaire.
® Uvéite Phacotoxique (ou phacolytique) : fuite de protéines du cristallin sans rupture capsulaire, souvent par une capsule vieillie et perméable d’une cataracte hypermûre.
V — PROPRIÉTÉS CELLULAIRE ET RENOUVÈLEMENT CRISTALLINIEN, HOMÉOSTASIE PROTÉIQUE ET MÉCANISMES DE LA CATARACTOGENÈSE :
Le cristallin est un tissu avasculaire en croissance continue dont la transparence dépend d’un délicat équilibre cellulaire et biochimique. L’ensemble des mécanismes qui entretiennent la transparence (production de nouvelles fibres, maintien de la solubilité protéique, systèmes antioxydants et pompes ioniques) forment une cascade protectrice ; la rupture de l’une de ces barrières, ou l’accumulation progressive de dommages (stress oxydatif, métabolique, génétique), conduit à l’agrégation protéique, à la perturbation de l’hydratation/ionique et, in fine, à la cataracte.
1. Renouvellement cellulaire :
- Épithélium antérieur : seul compartiment mitotique du cristallin. Les cellules de la zone germinative prolifèrent, migrent vers l’équateur et se différencient en fibres secondaires.
- Fibres cristalliniennes : cellules post-mitotiques qui, lors de la différenciation, perdent noyau et organites pour devenir transparentes. Les nouvelles fibres s’ajoutent en couches concentriques tout au long de la vie → croissance continue du cristallin.
- Conséquence : les fibres centrales sont les plus anciennes (noyau), les périphériques plus récentes (cortex) ; cette histoire spatiale influence la nature des lésions (sclérose nucléaire vs cataracte corticale).
2. Mécanismes de maintenance protéostatique et de réparation
- α-cristallines : préviennent l’agrégation et facilitent le repliement/protection des protéines sous stress.
- Systèmes d’élimination : ubiquitine-protéasome et l’autophagie éliminent les protéines endommagées/agrégées.
- Antioxydants enzymatiques :
GSH = tripeptide (glutamate-cystéine-glycine) présent en forte concentration dans le cristallin, principalement sous forme réduite (GSH).
Fonctions principales :
- Maintenir les groupes sulfhydryle (–SH) des protéines cristallines en état réduit, empêchant les ponts disulfures et l’agrégation protéique.
- Protéger les membranes et les pompes ioniques contre le stress oxydatif.
- Participer à l’élimination du H₂O₂ et des peroxydes lipidiques via la glutathion peroxydase (nécessite NADPH).
Métabolisme :
Le shunt pentose (voie des pentoses phosphates) produit le NADPH nécessaire au recyclage du GSSG (forme oxydée) en GSH.
💡 Note : Vieillissement / cataracte : diminution de GSH (et de l’activité des enzymes associées) est une des premières altérations dans la cataractogenèse ; augmentation du GSSG et oxydation des –SH entraînent la formation de liaisons disulfure et l’opacification.
- Pompes ioniques (Na⁺/K⁺-ATPase) et transporteurs d’acides aminés : maintiennent un gradient ionique et l’hydratation, assurant la stabilité osmotique.
3. Réponse au stress et voies conduisant à la cataracte
Les agressions (UV, radicaux libres, hyperglycémie, radiations, infections, agents tensioactifs) déclenchent plusieurs mécanismes délétères :
a. Stress oxydatif :
- Perte de GSH, accumulation de H₂O₂ et radicaux libres → oxydation des cystéines et formation de ponts disulfure (S–S) → modifications conformationnelles et agrégation des cristallines → diminution de la solubilité.
b. Dysrégulation calcique :
- Augmentation du Ca²⁺ intracellulaire active des calpaïnes (protéases Ca-dépendantes) → clivage de protéines structurelles et de membranes → perte d’intégrité des fibres et opacification.
c. Modifications post-traductionnelles (PTM) :
- Déamidation, glycation (formation d’AGEs en hyperglycémie), carbamylation, truncation, cross-linking, racémisation → altèrent le repliement, la solubilité et favorisent les agrégats à haut poids moléculaires HMW.
- Ces PTM sont cumulatives : certaines peuvent être réversibles/protectrices, d’autres irréversibles et pathogènes.
d. Stress osmotique métabolique :
Dans le diabète : accumulation de sorbitol via l’aldose réductase → entrée d’eau, gonflement des fibres, vacuolisation → cataracte sucrée (corticale).
e. Conséquences biochimiques :
- Perte de protéines solubles, augmentation de la fraction d’agrégats insolubles (water-insoluble fraction -WIF), perte d’ATP, altération enzymatique, perte d’inositol et d’acides aminés, déséquilibre ionique (↑Na⁺, ↓K⁺) → hydratation anormale et opacification.
f. Variations topographiques de la cataracte et mécanismes associés :
- Cataracte corticale : anomalies de perméabilité des fibres corticales → vacuoles, clivages. Souvent liées à des agents tensioactifs, diabète, radiation.
- Sclérose nucléaire : réticulage et déshydratation des fibres centrales anciennes → jaunissement/brunissement du noyau et augmentation de la densité optique.
g. Hypothèse de la charge cataractogène « cataractogenic loa hypothesis » :
- La perte de transparence résulte d’un fardeau cumulatif (load) de modifications moléculaires et cellulaires (PTM, agrégats, dommages membranaires, ADN).
- Il existe un tipping point : tant que la SRO et les mécanismes protecteurs tiennent, la transparence se maintient. Au-delà d’un seuil (taille/nombre d’agrégats, perte de chaperonne, stress massif), la diffusion augmente rapidement → cataracte clinique.
- Importance : pas seulement la quantité d’agrégats qui compte, mais leur nature, leur taille, leur organisation et le contexte biochimique.
h. Facteurs génétiques et catalyseurs métaboliques :
- Mutations des cristallines, connexines (Cx46, Cx50), ou enzymes antioxydantes peuvent provoquer cataractes congénitales/familiales.
- Hyperglycémie, urémie, exposition ionisante, médicaments et toxiques accélèrent la progression.
i. Implications cliniques et prévention :
- Prévention : contrôle glycémique, protection UV, réduction des expositions oxydantes, optimisation nutritionnelle (antioxydants) ; limiter médicaments ou agents cataractogènes si possible.
- Thérapies expérimentales : inhibiteurs d’aldose réductase, chaperones pharmacologiques, agents anti-agrégants, renforcement du GSH — en recherche active.
- Traitement définitif : chirurgie (phacoémulsification + implant). Les approches non-chirurgicales visent à retarder l’atteinte du tipping point.
Conclusion
Le cristallin, véritable lentille vivante, assure la réfraction et l’accommodation grâce à sa structure parfaitement organisée et à sa transparence exceptionnelle. Il s’agit d’un système dynamique : la production continue de fibres, la maintenance protéostatique et les défenses antioxydantes concourent à préserver l’homogénéité optique et la stabilité des cristallines.
La cataractogenèse résulte d’une cascade d’événements interconnectés — cellulaires, biochimiques et physiques — qui convergent vers la perte d’organisation locale des protéines (SRO) et la formation d’agrégats optiquement perturbants.
Comprendre ces interactions éclaire non seulement la physiologie du cristallin, mais aussi les stratégies préventives et thérapeutiques modernes visant à retarder ou corriger la perte de transparence, complémentaire à la chirurgie.
